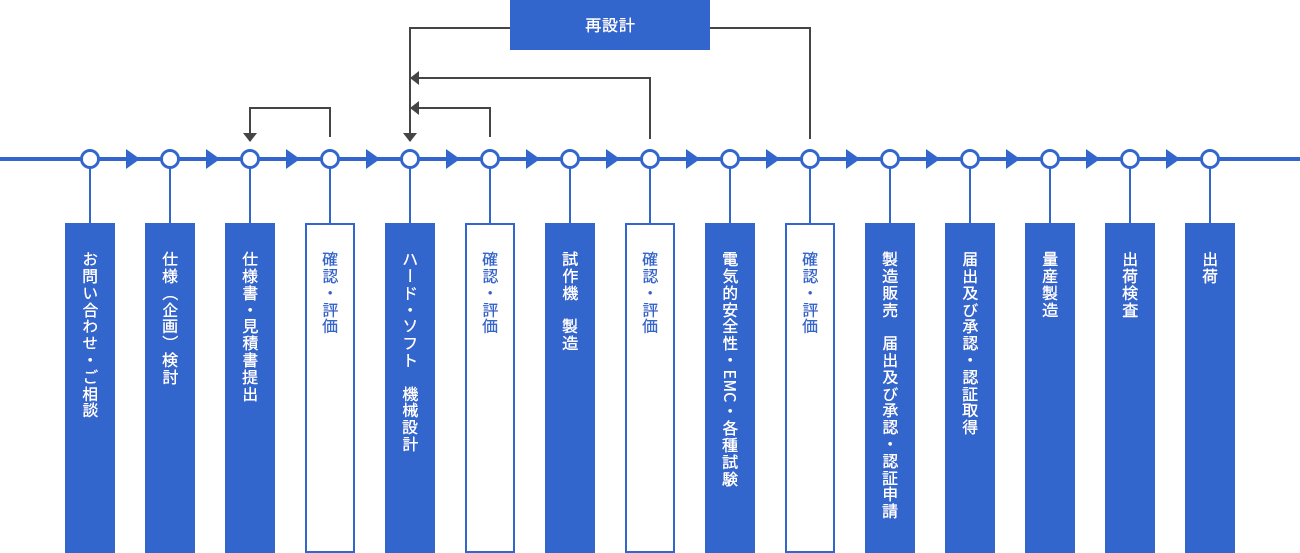
コスミックエムイーは創業からさまざまな医療機器の開発・製造を行っております。特に電子機器の心臓部にあたる電子制御部の開発を得意としており、なかでも、回路設計およびファームウェア設計においては多くのお客さまに高い評価をいただいております。また、電子医療機器以外での医療器具分野での開発・製造も行っております。
お客さまの要求事項を満たし、かつ、有効性や安全性に優れた製品づくりを行うことをモットーとしています。仕様変更などに迅速で柔軟に対応し、お客さまに心から満足していただける製品を目指します。

医療電子機器は一般の電子機器にくらべ、クリアしなければならない規制事項が多くあります。具体的には、電気的安全性、電磁的両立性(EMC)など、製品の分類に応じた特有の要求事項に適合していることを証明しなければなりません。
弊社は医療電子機器認証および承認基準として要求されているJIS T0601-1などの規格に精通しています。医療電子機器の設計開発の際は基準に適合するよう、十分に考慮し、工程を進めていきます。

医療機器製造業者として製品を完成まで製造し、販売業者に出荷することが可能です。医療機器は公的に許可を受けている事業者でないと製造をおこなうことができません。弊社では薬事法および国際規格(ISO)に準拠した製造・品質管理体制を完備し、医療機器製造に取り組んでいます。
また、医療機器業許可のもと、クラスⅢ(高度管理医療機器)に分類される手術用医療機器も製造しています。

製品の品質保証の確保を最重要課題とし、医療機器の製造・管理体制の国際規格であるISO13485:2016をベースに管理体制を構築し、運用しています。薬事法でも医療機器製造業者はこの規格に準拠して制定されたQMS省令に適合することを要求しております。
弊社では、部材の調達から製品にかかわるすべての工程にこの規格を運用し、品質マネジメントシステムを構築し、国際的な第三者認証機関よりISO13485の認証を取得しております。

医療機器を市場で販売するためにはその医療機器の販売承認または認証を取得しなければなりません。弊社では第1種医療機器製造販売業許可を有しており、クラス分類におけるクラスⅣ(高度管理医療機器)までの医療機器の製造販売申請を行うことが可能です。
お客さまが販売業のみの許可を取得している場合や、都合により自ら認証申請を行えないなどの事情がある場合でも、弊社で認証申請を行い認証取得後にお客さまへOEM供給することが可能です。弊社では迅速に認証が得られるよう、書類作成から当局との折衝まで、幅広く対応します。

医療にかかわる新技術の研究開発や新事業の創出を図ることを目的とし、
大学などの教育・研究機関、民間企業の医療関係者と工学関係者が連携することを言う。
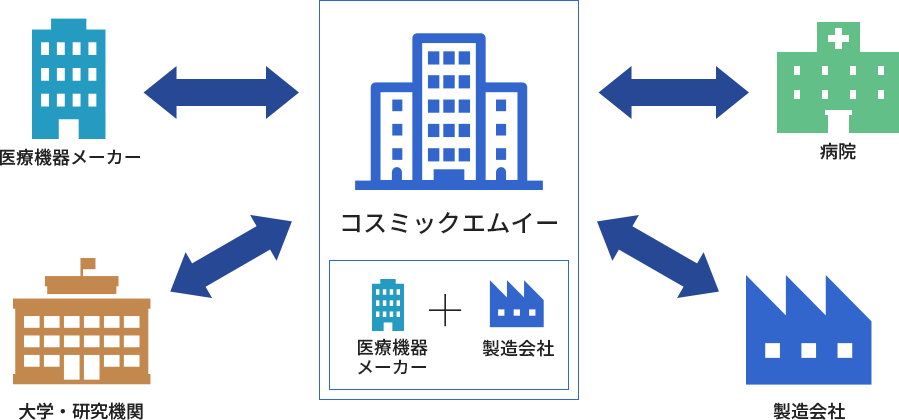
医学部や医療機関などの医学分野には「こんな機能があればいいのに」「ここをこうすればもっとよくなるのに」といったニーズが至る所にあります。一方、工学分野の理工学部やものづくり企業はそれぞれが独自の技術やノウハウ。シーズを持っております。
そこの両者の連携が上手く取れていないのが日本の現状です。
今は国が国策として国産の医療機器の開発を支援し、輸出まで持っていけるような製品を生み出せるような土壌が出来つつあります。
ただ医療業界とは業許可の取得なども含め参入が難しい分野でもあります。当社では様々な事情で参入することをためらっている企業のサポートをいたします。
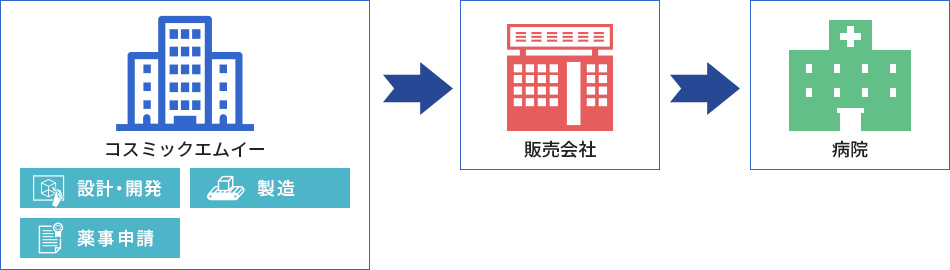
CMEが医療機器の設計開発を行い、医療機器製造販売業者として薬事申請します。量産も弊社が医療機器製造業者として行い、医療機器販売業者に製品を販売します。
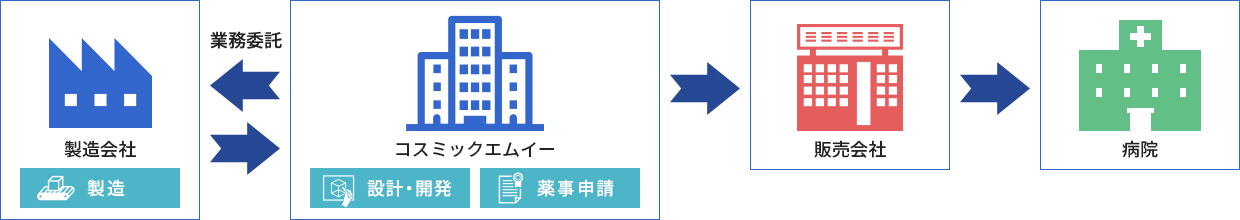
CMEが医療機器の設計開発を行い、医療機器製造販売業者として薬事申請を行います。量産製造は医療機器製造業者へ委託し、医療機器販売業者への販売はCMEが担う形になります。
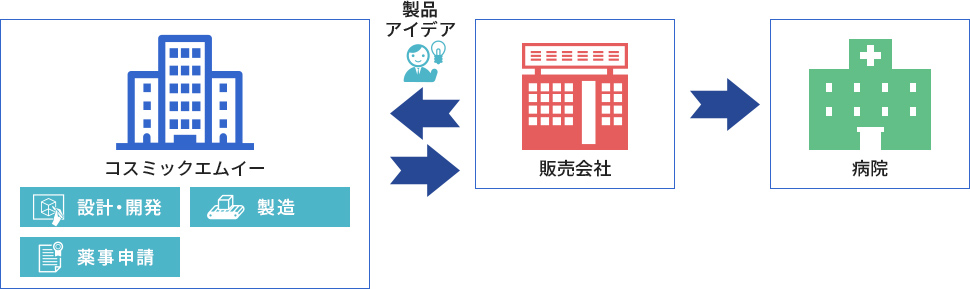
医療機器販売業者から製品化の開発・製造の依頼にもとづき、CMEが設計開発を行います。医療機器製造販売業者として薬事申請をし、量産についても、弊社が医療機器製造業者として請け負います。製品は特定の医療機器販売業者に専属販売します。
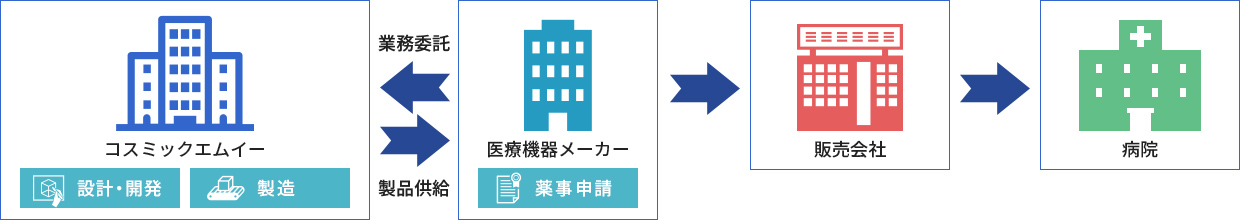
医療機器製造販売業者から開発・製造を受託し、医療機器の設計開発を行います。依頼元が完成品を医療機器製造販売業者として薬事申請を行い、CMEは医療機器製造業者としてOEM供給します。
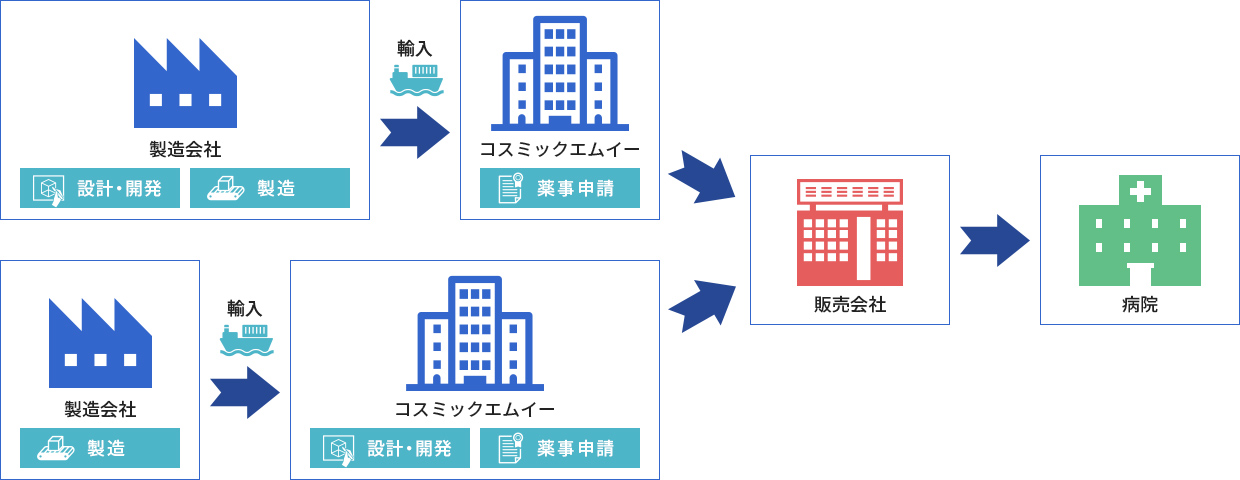
医療機器製造販売業者としての輸入を行う海外の医療機器メーカーの製品に対し、弊社が医療機器製造販売業者として薬事申請を行い、CMEが輸入元になります。海外の医療機器への薬事代行を行います。